滴水成冰的原理是物体从液态变成固态,需要满足两个条件:一是水冷却到结晶温度,即零摄氏度;二是依靠细小结晶核结晶。当水从当前温度向结晶温度降温时,与细小结晶核发生接触时,水会慢慢结成冰。
滴水成冰的过程就是滴水继续从热状态向冷状态降温时,把液态水依次转换成气态、固态水,较厚的液态水会慢慢结成冰,冰的厚度越来越大。 滴水成冰其实就是凝固现象,需要有两大条件,一个是温度非常低,另一个条件是物体需要有相应的凝固点。 在温度低至零摄氏度以下,水分子失去能量,运动减慢,整齐有序的排列在一起做固定的振动运动,水就成冰了。
点水成冰是一个常见的现象,这种现象是可以通过实验来进行***的,以此来不断的重现,而能够实现点水成冰现象的出现是由于过饱和溶液因不稳定性而产生的。
一、点水成冰的原理
点水成冰的出现是由于过饱和溶液因不稳定性而产生的。醋酸钠的热饱和溶液在不受扰动下冷却,结晶作用往往不会发生。这种溶液称为过饱和溶液,是一种介稳体系,本身虽然是不稳定体系,但是尚能存在。当搅动此溶液或加入溶质的“籽晶”,即能析出过量溶质的结晶。
二、点水成冰现象的反复重现实验步骤
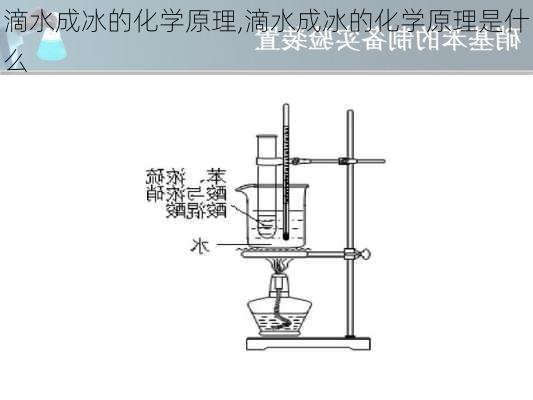
首先准备仪器与材料。然后溶解醋酸钠晶体,在250毫升烧杯中放入醋酸钠晶体(NaAc·3H2O)60克并注入蒸馏水40毫升,然后通过水浴加热的方式直至晶体全部溶解,再持续几分钟后,取出盛有溶液的烧杯,静置冷却到室温。最后,点水成冰出现,用玻棒伸入溶液内轻轻摩擦一下杯壁或搅动一下溶液或向溶液内投入一粒醋酸钠晶体作为“籽晶”,顿时溶液内会析出针状结晶,并迅速遍及整个烧杯底部,好像结成了“冰块”的样子。

三、实验中注意事项
溶液在冷却过程中,切记不能受震动或粘上灰尘!而且醋酸钠用后要进行回收。在实验的所用材料上,如用硝酸钠、硫酸钠晶体(NaSO4·10H2O)都是可以进行同样的实验。如果直接用硫代硫酸钠(俗称海波:Na2S2O3·5H2O)进行实验时,要小心加热,利用其结晶水溶解制成过饱和溶液,实验现象将会更加明显。
原理:这是过饱和溶液不稳定性的实验。醋酸钠的热饱和溶液在不受扰动下冷却,结晶作用往往不会发生。这种溶液称为过饱和溶液,是一种介稳体系(不稳定体系,但尚能存在)。当搅动此溶液或加入溶质的“籽晶”,即能析出过量溶质的结晶。
当气温低于-40℃时,还不足以实现“过水成冰”,泼出去的无数个水滴外层能迅速结冰,但内部仍是水,水滴完全冻结需要一定时间,还有一种特殊情况,就是冷空气翻过雪山携带大量冰核,有可能会出现泼水成冰